近日,我校生命科学学院王伟武老师课题组在膜蛋白结构生物学研究方面取得重要进展,相关研究论文"Cross-protomer interaction with the photoactive site in oligomeric proteorhodopsin complexes”以南京农业大学为第一通讯作者单位,青年教师冉婷婷和博士研究生郜彦彦等为第一作者,发表在生物物理学排名第一的杂志Acta Cryst. (2013). D69, 1965-1980(IF 14.1)上。由于PR蛋白结构的新颖性以及重要性,该论文被杂志编辑选为封面论文进行发表(http://journals.iucr.org/d/issues/2013/10/00/issconts.html )。
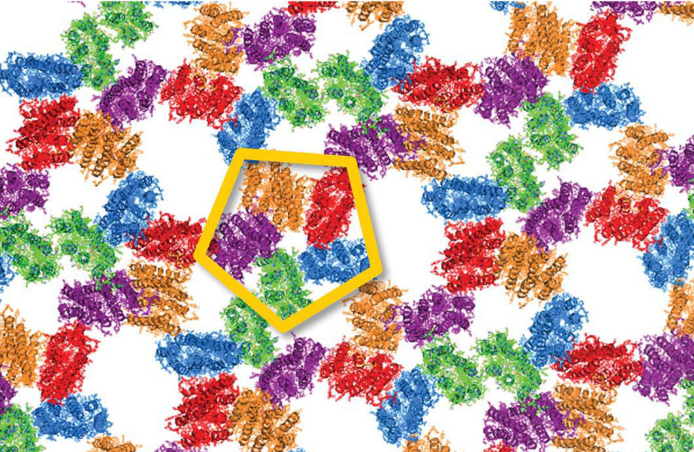
封面论文用图:蓝光吸收性 Proteorhodopsin 在一型膜蛋白晶体中形成 的环状五聚体
Proteorhodopsin是一类广泛存在于海洋及淡水微生物中的光驱动质子泵,对于水体中能量的循环尤其是海洋中的能量循环具有重要的作用,但目前有关质子转运机制的研究较少。在该论文中作者解析了两种来源于海洋微生物的Proteorhodopsin(PR)家族蛋白的三维晶体结构,发现Proteorhodopsin与它的同源蛋白bacteriorhodopsin(bR)在结构上存在明显的差异。PR蛋白一个重要的特征就是相邻的PR分子间存在一种特殊的相互作用,这种相互作用由保守的His75和相邻分子的Trp34形成,并可能与分子间的协同作用有关;其次PR的质子释放基团明显不同于bR;另外由于没有发现在bR中与质子转运相关的一个水分子,因此推测PR的质子转运机制与bR明显不同。

封面论文用图:蓝光吸收性 Proteorhodopsin 在一型膜蛋白晶体中形成 的环状五聚体
Proteorhodopsin是一类广泛存在于海洋及淡水微生物中的光驱动质子泵,对于水体中能量的循环尤其是海洋中的能量循环具有重要的作用,但目前有关质子转运机制的研究较少。在该论文中作者解析了两种来源于海洋微生物的Proteorhodopsin(PR)家族蛋白的三维晶体结构,发现Proteorhodopsin与它的同源蛋白bacteriorhodopsin(bR)在结构上存在明显的差异。PR蛋白一个重要的特征就是相邻的PR分子间存在一种特殊的相互作用,这种相互作用由保守的His75和相邻分子的Trp34形成,并可能与分子间的协同作用有关;其次PR的质子释放基团明显不同于bR;另外由于没有发现在bR中与质子转运相关的一个水分子,因此推测PR的质子转运机制与bR明显不同。

